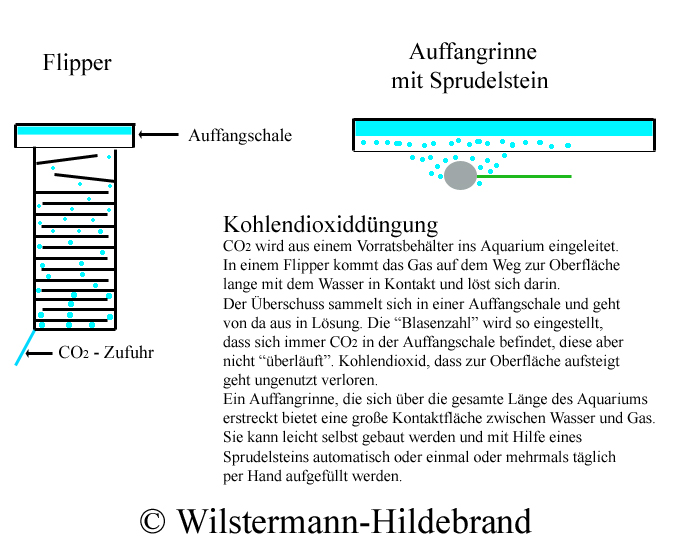
Die Auffangschale befindet sich immer unter Wasser. Der Wasserdruck trägt zur besseren Lösung des Gases bei.

Kohlenioxiddüngung gilt bei vielen Aquarianern als Wundermittel für optimalen Pflanzenwuchs.
Tatsächlich lässt sich das Pflanzenwachstum auch durch die Zufuhr von Kohlendioxid steigern. Das ist aber nicht unbedingt sinnvoll.
Pflanzen leiden im Aquarium nicht unter "Kohlendioxidmangel". Um ihren Bedarf zu decken, reichen Konzentrationen von etwa 0,1 mg CO2 pro Liter Wasser aus (Kompensationspunkt).
Dieser Grundbedarf ist in einem Aquarium mit biologischem Filter und einigen Tieren immer gedeckt.
Die Sättigung - also der Punkt, an dem die Pflanzen mehr Kohlendioxid bekommen, als sie aufnehmen können - liegt bei Lichtsättigung (35.000 Lux) zwischen etwa 10 (pH 8) und 26 mg/l (pH 4).
Bei einer geringerer Belichtung liegt der Sättigungspunkt darunter. Den Pflanzen mehr als 15 mg/ CO2 anzubieten ist also überflüssig, weil sie mehr ohnehin nicht nutzen können.
Eine Steigerung des Lichtangebots und der Kohlendioxidzufuhr sind immer mit einem erhöhten Nährstoffbedarf verbunden.
Wenn Ihr mit zusätzlichen Kohlendioxid düngt und es dadurch nicht mehr der begrenzende Faktor ist, wird ein anderer Nährstoff das Wachstum begrenzen (Minimumgesetz von Liebig).
Dann treten Mangelerscheinungen, wie Chlorosen, Verkrüppelungen oder das Absterben von Pflanzenteilen auf.
Dann müssen die fehlenden Nährstoffe ergänzt werden, bis wieder Kohlendioxid der begrenzende Faktor ist.
Ist Kohlendioxid der begrenzende Faktor für den Pflanzenwuchs und nicht andere Nährstoffe wie Eisen oder andere Mikronährstoffe,
treten keine Mangelsymptome auf (siehe dazu Pflanzenernährung).
Es ist unnötig mehr als 15 mg/l CO2 im Aquarienwasser zu haben. Höhere Konzentrationen nutzen den Pflanzen nichts, können aber für Fische und Garnelen gefährlich werden.
Kohlenstoffdioxid (CO2) ist ein farbloses Gas, das zu 0,039 Vol% (390 ppm) Bestandteil
unserer Erdatmosphäere ist. Es entsteht bei der Verbrennung von
Kohlenstoff haltigen Materialien (Holz, Kohle, Benzin etc.) und bei der
Zellatmung aus der Umwandlung von Zucker. Kohlendioxid ist
wichtig für das Leben auf der Erde. Es dient allen Pflanzen als
Kohlenstoffquelle. Mit Hilfe der Sonnenenergie gewinnen sie aus
Kohlenstoffdioxid und Wasser energiehaltige organische Verbindungen
(Zucker und Stärke). Diese sind die Grundlage der meisten
biologischen Stoffwechselprozesse und werden von fast allen Lebewesen
als Lebensgrundlage genutzt. Weil die Pflanzen in der Lage sind die
ersten chemischen Substanzen für Nahrungsketten quasi aus dem
Nichts zu produzieren, werden sie als Primärproduzenten
bezeichnet.
In der Atmosphäre sammelt sich Kohlendioxid durch die Verbrennung
fossiler Rohstoffe (Kohle und Öl) immer stärker an. Seit
Jahrmillionen gespeichertes Kohlendioxid wurde in wenigen Jahrzehnten
freigesetzt. Mehr als die Pflanzen auf der Erde, die zeitgleich durch
Abholzung der Wälder und Desertifikation (Ausbreitung von
Wüsten) in ihrer Masse abnahmen wieder aufnehmen konnten. Dadurch
ist die Kohlendioxidkonzentration in der Atmosphäre sangestiegen.
Eine Folge davon ist die globale Erwärmung.
Im Aquarium haben wir oft das gegenteilige Problem. Kohlendioxid ist
nicht immer im ausreichenden Maße vorhanden. Das Gas löst
sich
recht gut in Wasser. In den abgeschlossenen Becken ist der
Verbrauch aber manchmal höher als die Produktion durch die Atmung
von Fischen, Krebsen, Garnelen, Schnecken und Bakterien. Dann muss man
es manchmal künstlich zuführen. Pflanzen nutzen Kohlendioxid
als
Quelle für Kohlenstoff und benötigen es zum Wachsen. Tiere
können aber nur begrenzte Mengen an CO2 vertragen. Es
ist also wichtig das richtige Maß im Aquarium zu finden.
Fische atmen Sauerstoff ein und Kohlendioxid aus. Pro Gramm
Lebendgewicht gibt ein Fisch etwa 15 bis 40 mg CO2
täglich ab (Krause 1998). Der Austausch der Gase zwischen Blut und Wasser erfolgt an den Kiemen.
Durch Diffusion bewegen sich die Gasmoleküle jeweils in das Medium, dass
die geringere Konzentration aufweist. Das Fischblut in den Kiemen
enthält wenig Sauerstoff und viel Kohlendioxid, das Wasser im Vergleich dazu viel
Sauerstoff und wenig Kohlendioxid. So wird Sauerstoff aufgenommen und CO2
abgegeben. Im Kiemenblut wird der Sauerstoff an die roten
Blutkörperchen gebunden. Im Gegenzug löst sich das Kohlendioxid davon und
diffundiert aus dem Blut ins Wasser. Der Sauerstoffgehalt im Aquarium darf also an sich
nicht zu niedrig sein und ein zu hoher Kohlendioxidgehalt im Aquarienwasser
behindert die Abgabe von CO2 über die Kiemen und macht eine
Sauerstoffaufnahme unmöglich. Wie viel CO2 für Fische kritisch ist,
hängt vor allem von der Fischart ab. Fische aus schnell strömenden, sauerstoffreichen,
kühleren Bächen sind weniger tolerant als solche aus stehenden oder langsam
fließenden Gewässern. Bei einer guten Sauerstoffversorgung wird mehr
Kohlendioxid vertragen. Verlässliche Messungen oder Studien zur CO2-Toleranz
von tropischen Zierfischen gibt es kaum. Es ist also schwierig Grenzwerte
für Kohlendioxid im Aquarium anzugeben. Die errechneten CO2-Gehalte
natürlicher Gewässern liegen in etwa 85 % der Fälle unter 20 mg/l.
Diese Schätzung basiert auf den von Kasselmann (2010) angegebenen CO2-Werten in der Tabelle mit den Wasserwerten
verschiedener Wasserpflanzenbiotope (S. 566-573). Die Hartwasserflüsse in Thailand mit > 40 mg CO2 /l sind dabei nicht
berücksichtigt.
Etwa 20 bis 25 mg/l CO2 sind bei ausreichendem Sauerstoffangebot für Aquarienfische und
Wirbellose unproblematisch. Pflanzen erreichen bei diesen Werten bereits ihren Sättigungspunkt.
Eine Steigerung über diesen Wert hinaus, fördert ihr Wachstum also nicht mehr.
Pflanzen atmen ebenfalls und benötigen dazu Sauerstoff. Sie atmen Kohlendioxid aus. Tagsüber betreiben sie aber Fotosynthese
und ihr Verbrauch an CO2 ist dann größer als ihr CO2-Ausstoß, wenn sie ausreichend Licht zur Verfügung haben.
Die CO2-Kompensationspunkte sind bei den Pflanzenarten unterschiedlich und ändern sich in Abhängigkeit von den
Umweltbedingungen. Bei allen Wasserpflanzenpflanzen liegen sie jedoch weit unter den normalen CO2-Mengen
in Aquarien. Der minimale Bedarf an Kohlendioxid ist also immer gedeckt. CO2-Sättigungspunkte oder die Konstanten der
halbmaximalen Fotosyntheserate (Km) sind ebenfalls sehr variabel und werden stark
vom Lichtangebot, dem pH-Wert und der Temperatur beeinflusst.
CO2-Kompensationspunkte verschiedener
submerser Pflanzen in Abhängigkeit von der Temperatur und der Tageslänge
(nach Salvucci & Bowes 1981 und Hough & Wetzel 19781)
| 30 °C/14-h | 12 ° C/ 10-h |
CO2-KP in mg/l |
|
| |
µl CO2 /l |
µl CO2 /l |
30 °C/14-h / 12 ° C/ 10-h |
|
Höhere Pflanzen |
|
|
|
| C. caroliniana |
10 |
82 |
0,0198 / 0,1621 * |
|
C. demersum |
26 |
82 |
0,0514 / 0,1621 * |
| E. densa | 17 | 43 | 0,0336 / 0,0850 * |
| H. verticillata | 10 |
84 |
0,0198 / 0,1661 * |
| M. brasiliense |
11 |
62 |
0,0218 / 0,1226 * |
| M. heterophyllum |
10 |
- |
0,0198 / - * |
|
M. spicatum |
12 |
83 |
0,0237 / 0,1640 *> |
| Najas flexilis 1 |
|
|
0,08 – 0,5 |
| P. palustris |
24 | 58 | 0,0474 / 0,1147 * |
| Moose | |
|
|
| F. cf manateensis |
16 | 50 | 0,0316 / 0,0988 * |
| Algen |
|
|
|
| Nitella sp. |
6 |
110 | 0,0119 / 0,2175 * |
* Die Werte dienen zur besseren Vergleichbarkeit mit der aquaristisch üblichen Messgröße. Sie sind umgerechnet mit einer CO2-Masse von 1,977 mg/ml.
CO2-Konstante der Halbmaximalen Fotosyntheserate und CO2-Sättigungswerte nach Van et
al. 1976, umgerechnet in mg/l CO2. Die Werte wurden bei Lichtsättigung (ca. 35 klux) 25 °C und einer
Tageslänge von 12 Stunden bestimmt.
| Halbmaximale Fotosyntheseleistung bei pH 4 [mg CO2 /l ] |
Halbmaximale Fotosyntheseleistung bei pH 8 [mg CO2 /l ] |
Sättigungswert bei pH 4 [mg CO2 /l ] |
Sättigungswert bei pH 8 [mg CO2 /l ] |
|
| Ceratophyllum demersum | 7,26 | 4,16 | ~ 26,4 | ~ 11,88 |
| Hydrilla verticillata | 7,48 | 3,96 | ~ 25,5 | 18,5 |
| Myriophyllum spicatum | 6,6 | 3,3 | ~ 26,0 | ~ 15,4 |
Dem Kohlendioxidgehalt des Wassers müssen immer auch eine
ausreichende Lichtmenge und genug Nährstoffe gegenüber
stehen, damit die Pflanzen das Angebot voll nutzen können. Auch die Temperatur
spielt eine wichtige Rolle. Die Temperatur für die maximale CO2-Fixierung
beträgt bei Hydrilla verticillata 36,5 °C,
bei Myriophyllum spicatum 35 °C und bei Ceratophyllum demersum 28,5
°C. Es ist also kaum möglich, dass die Pflanzen ihre Möglichkeiten im Aquarium voll ausschöpfen.
Für die meisten Aquarienpflanzen gibt es keine
Untersuchungen zum CO2-Bedarf. Bei Amano´s
"Pflanzenparadiese unter Wasser" (1994) sind die
CO2-Werte bei den einzelnen Layouts mit > 10 bis 23 mg/l
angegeben. Bei den meisten seiner Aquarien sind es etwa 15 mg CO2
pro Liter. Bei diesem Wert lassen sich die meisten Pflanzen
einschließlich Mayaca fluviatilis, Rotala wallichi, Hemianthus
micranthemoides, Glossostigma elatinoides, Eleocharis-Arten und Riccia
fluitans gut kultivieren. Cryptocorynen, Wasserfreund-Arten und Farne benötigen weniger. Je nach
Lichtangebot, Düngung und Pflanzenbesatz braucht man im Aquarium für ein optimales
Pflanzenwachstum zwischen 10 und 25 mg CO2 pro Liter Wasser. Diese Werte sind
für Fische unbedenklich.
Kohlendioxid gelangt durch die Atmung der Aquarienbewohner ins
Wasser. Krause (1998) gibt an, dass ein Fisch pro Gramm
Lebendgewicht etwa 15 bis 40 mg CO2 täglich ab
gibt. Besonders viel Kohlendioxid entsteht bei der Zersetzung von
organischem Material. Aus einem 1 Kubikzentimeter Flockenfutter (ca.
0,25 g) werden 700 mg CO2 freigesetzt. Es wird durch die
zersetzenden Würmer, Pilze und Bakterien ausgeatmet. Im Bodengrund
und im Filter ist der Kohlendioxidgehalt darum höher als im freien
Wasser.
Bereits zu Beginn des 20. Jahrhunderts wurde vermutet, dass Wasserpflanzen neben gelöstem Kohlendioxid auch Kohlenstoff aus
Bicarbonaten nutzen können. Dabei spalten die Pflanzen Bikarbonate auf und es bildet sich eine
Schicht aus Hydrogenkarbonat auf den Blättern. Dieser Vorgang wird
als Biogene Entkalkung bezeichnet.
1910 versuchte Udo Angelstein das in seiner Dissertation
nachzuweisen. Er benutzte dazu als Maß von den Pflanzen
produzierte
Sauerstoffbläschen. Da diese Bestimmungsmethode sehr ungenau ist, wurde das Ergebnis noch
in den 70er Jahren angezweifelt. Eine
amerikanische Studie von 1988 hat diese Ergebnisse jedoch bestätigt. Beispielsweise konnte keine Wachstumssteigerung
bei Hydrilla erzielt
werden, wenn zusätzlich zu Bicarbonaten Kohlendioxid zugeführt wurde. Bei niedrigem Carbonatgehalt wirkte sich das CO2
stark aus. Bei Elodea und Potamogeton
zeigte Kohlendioxidzugabe bei geringem Carbonat-Gehalt keine Wirkung. Bei erhöhter Fotosyntheserate gab es
Verschiebungen im Reaktionsgleichgewicht zwischen Calciumcarbonat und freiem
CO2. Offenbar ist es für die Pflanze von Vorteil auf die Carbonate im Wasser zurück zu greifen, da
der Kohlendioxid-Anteil in Abhängigkeit von Wasserbewegung und Temperatur schwankt, der Carbonat-Gehalt sich aber kaum ändert. Die Lösung des Carbonats erfolgt
durch die Aussscheidung von Wasserstoffionen, die den pH-Wert absenken.
Man kann den CO2-Gehalt aus dem pH-Wert und der Carbonathärte ableiten. Diese
Zahlen stellen aber nur Richtwerte dar. Bei Nitratwerten über 50 mg/l und durch Zusatz von pH-Senkern oder Torffiltern wird der ph-Wert
gesenkt ohne, dass entsprechend CO2 vorliegt. Die meisten
Aquarienpflanzen lassen sich bei diesen Härtegraden und pH-Werten
problemlos kultivieren.
| °dKH \ pH | 6,4 | 6,6 | 6,8 | 7,0 | 7,2 | 7,4 | 7,6 | 7,8 |
| 2 | 25 | 16 | 10 | 7 | 4 | 3 | 2 | 1 |
| 4 | 50 | 32 | 20 | 13 | 8 | 5 | 3 | 2 |
| 6 | 75 | 50 | 30 | 20 | 12 | 8 | 5 | 3 |
| 8 | 100 | 65 | 40 | 25 | 16 | 10 | 6 | 4 |
| 10 | 130 | 80 | 50 | 32 | 20 | 13 | 8 | 6 |
| 12 | 150 | 100 | 60 | 40 | 24 | 15 | 10 | 6 |
| 14 | 180 | 115 | 70 | 45 | 28 | 18 | 11 | 7 |
| 16 | 200 | 130 | 80 | 50 | 32 | 20 | 12 | 8 |
| 18 | 230 | 145 | 90 | 58 | 36 | 23 | 14 | 9 |
| 20 | 250 | 160 | 100 | 60 | 40 | 25 | 16 | 10 |

Durch die künstliche Zufuhr von Kohlendioxid, kann die biogene Entkalkung vermeiden und die Karbonathärte erhalten
werden. Versuche haben aber gezeigt, dass etwa 90% des CO2 sofort aus dem
Wasser entweicht, wenn es direkt eingeleitet wird. Es steigt als Blasen an die
Wasseroberfläche. Der Einsatz einer Auffangschale oder Auffangrinne ist darum sinnvoll. Das Kohlendioxid
sammelt sich in der Schale und bleibt so on Kontakt mit dem Wasser. Es
wird mehr im Wasser gelöst und die Ausnutzung des zugeführten
Gases ist effektiver (siehe Paffrath 1979, S. 145).
Den pH-Wert mit Hilfe von Kohlendioxid zu senken ist nur in begrenztem
Maße möglich. MÖchte man beispielweise den pH-Wert bei einer Karbonathärte von 4 von 7,2 auf 6,8 senken, braucht man den
Kohlendioxidgehalt nur um 12 mg/l zu erhöhen. Bei einer Karbonathärte von 8 braucht man dazu bereits eine Erhöhung zm
34 mg/l und überschreitet 30 mg/l im Wasser, so dass es zur Schädigung von Tieren im Aquarium kommen kann.
Oft fragen Aquarianer nach der notwendigen "Blasenzahl" als Maß für die Kohlendioxidzufuhr. Diese Frage ist ganz einfach zu
beantworten: Es wird soviel CO2 eingeleitet wie im Wasser in der gleichen Zeit gelöst werden kann. Die Auffangschale über
dem Flipper soll Gas enthalten, aber nicht so voll sein, dass es in Blasen daraus aufsteigt. CO2, das an die Oberfläche
steigt, geht ungenutzt verloren.
Jedesmal, wenn jemand davon spricht sein Pflanzenwachstum zu "verbessern", stellt sich die Frage, wie man gutes Pflanzenwachstum definiert. Für manch einen Aquarianer ist es ein tolles Erlebnis vor seinem Aquarium zu sitzen und sich schöne, artgerecht gefärbte Pflanzen mit unbeschädigten Blättern anzusehen. Er mag es einmal die Woche ein Paar Blätter abzuzupfen. Andere Aquarianer mögen "Leistung" und messen ihren Kulturerfolg daran, wieviel Pflanzenmasse ihr Aquarium in der Woche produzieren kann. Die Aquarianer aus der ersten Gruppe haben meist ein Licht limitiertes Aquarium, dass ohne viel zusätzlichen Dünger und ohne Kohlendioxiddüngung auskommt. Sie pflegen, die Pflanzen deren Lichtansprüche gering bis Mittel sind. In der zweiten Gruppe muss ständig die Nährstoffzufuhr reguliert werden, da immer irgendein Nährstoff oder Kohlendioxid das Wachstum begrenzt oder zu Mangelsymptomen führt.
| Licht limitiert (0,5 W/l) 1 |
Starklichtbecken 2 |
|
| Erntemenge an Pflanzenfrischmasse pro Liter im Monat |
2 g |
etwa
6,7 g |
| Nährstoffentzüge durch die Pflanzenmasse = notwendige Düngermenge* |
||
| Stickstoff (N): 1,5 - 2 % in der Trockenmasse |
3 - 4 mg N = 9 - 12 mg Nitrat |
10,05 - 13,4 mg N = 31,5 - 40,2 mg Nitrat |
| Phosphor (P) : 0,2 - 0,5 % in der Trockenmasse |
0,4 - 1 mg P = 1,27 - 3,17 mg Phosphat |
1,34 - 3,35 mg P = 4,25 - 10,62 mg Phosphat |
| Kalium (K): 1 - 3 % in der Trockenmasse |
2 - 6 mg K+ |
6,7 - 20,1 mg K |
| Calcium (Ca): 0,5 - 1 % in der Trockenmasse |
1 - 2 mg Ca+ |
3,35 - 6,7 mg Ca+ |
| Magnesium (Mg): 0,2 - 0,4 % in der Trockenmasse |
0,4 - 0,8 mg Mg 2+ |
1,34 - 2,64 mg Mg 2+ |
| Eisen (Fe): 0,01 - 0,03 % in der Trockenmasse |
0,02 - 0,06 mg Fe |
0,067 - 0,20 mg Fe |
Quellen:
1 G. Kassebeer (2009): Leserbrief.- Aqua Planta 2-2009, 75
2 H.-G. Kramer (2009): Pflanzenaquaristik á la Kramer, Tetra Verlag GmbH
* Ausgehend von einem durchschnittlichem Wassergehalt von 90%
(entspricht dem von Elodea)

Literatur:
R. A. Hough, R. G. Wetzel (1978): Photorespiration and CO2 compensation point in Najas flexilis.- Limnol. Oceanogr., 23(4), 719-724
C. Kasselmann (2010): Aquarienpflanzen.- 3. Auflage, Ulmer Verlag
H.-J- Krause (1998): Handbuch Aquarienwasser.- 4. Auflage,Bede-Verlag
S. C. Maberly (1985): Photosynthesis bie Fontinalis antipyretica - I. Interaction between photon irridiance, concentration of carbon dioxid and temperature.- New Physiologist, 100, 127 - 140
K. Paffrath (1979): Bestimmung und Pflege von Aquarienpflanzen.- Landbuch-Verlag GmbH, Hannover
M. E. Salvucci, G. Bowes (1981): Induction of Reduced Photorespiratory Activity in Submersed and Amphibious Aquatic Macrophytes.- Plant Physiol. 67, 335-340

© Wilstermann-Hildebrand 2000 - 2025
Impressum
Datenschutzerklärung